阿爾茨海默病(AD)的特征是進(jìn)行性認(rèn)知功能下降、記憶力減退及日常生活能力喪失。盡管已有大量研究,目前仍缺乏能夠有效延緩或逆轉(zhuǎn)疾病進(jìn)程的治療手段。近年來(lái),基于干細(xì)胞的療法因其再生潛能與病理調(diào)節(jié)能力而受到廣泛關(guān)注。其中,自體血液來(lái)源干細(xì)胞(ABSCs)因來(lái)源于患者自身,可避免免疫排斥風(fēng)險(xiǎn),在AD治療中展現(xiàn)出良好的應(yīng)用前景。

為系統(tǒng)評(píng)估ABSCs聯(lián)合生長(zhǎng)因子治療中重度AD的安全性、有效性及其潛在機(jī)制,本研究開(kāi)展了一項(xiàng)前瞻性臨床探索,相關(guān)成果已在《Molecular Neurobiology》期刊上發(fā)表,標(biāo)題為“自體血液來(lái)源干細(xì)胞聯(lián)合生長(zhǎng)因子治療中重度阿爾茨海默病療效:一項(xiàng)臨床試驗(yàn)”[1]。

本研究提出以下假設(shè):ABSCs與生長(zhǎng)因子聯(lián)合應(yīng)用可通過(guò)激活PI3K/Akt和MAPK/ERK等關(guān)鍵信號(hào)通路,促進(jìn)神經(jīng)元存活、增強(qiáng)突觸可塑性,從而改善認(rèn)知功能并延緩疾病進(jìn)展。同時(shí),研究也全面評(píng)估了該療法在臨床應(yīng)用中可能遇到的不良事件、免疫反應(yīng)及其他潛在風(fēng)險(xiǎn),以驗(yàn)證其安全性與可行性。
初步結(jié)果顯示:ABSCs聯(lián)合生長(zhǎng)因子治療顯著改善了患者的認(rèn)知功能,降低了腦內(nèi)淀粉樣斑塊負(fù)荷,并在神經(jīng)影像學(xué)中觀察到積極的結(jié)構(gòu)與代謝變化。與異體干細(xì)胞相比,自體干細(xì)胞治療進(jìn)一步降低了免疫排斥風(fēng)險(xiǎn),安全性更高。此外,生長(zhǎng)因子的協(xié)同使用有助于增強(qiáng)干細(xì)胞療效,與既往研究結(jié)論一致。本研究為ABSCs聯(lián)合生長(zhǎng)因子治療中重度AD提供了初步的臨床證據(jù),支持其具有值得深入探索的治療潛力。
方法與標(biāo)準(zhǔn)
本研究采用了一項(xiàng)嚴(yán)謹(jǐn)且多維度的方法,旨在系統(tǒng)評(píng)估自體干細(xì)胞聯(lián)合生長(zhǎng)因子治療中重度阿爾茨海默病的療效與機(jī)制。具體方法可概括如下:
研究設(shè)計(jì)與實(shí)施:本研究為一項(xiàng)前瞻性、單中心、探索性隨機(jī)對(duì)照試驗(yàn)。采用計(jì)算機(jī)生成的區(qū)組隨機(jī)化方法(區(qū)組大小為4)將合格受試者分組,并通過(guò)順序編號(hào)的密封不透明信封實(shí)現(xiàn)分配隱藏。盡管對(duì)患者和治療醫(yī)師未設(shè)盲(出于治療操作需要),但為最大程度減少測(cè)量偏倚,研究采用了評(píng)估者盲法,即所有進(jìn)行認(rèn)知評(píng)估、神經(jīng)影像判讀和實(shí)驗(yàn)室分析的研究人員均對(duì)分組信息不知情。
研究對(duì)象與干預(yù)措施:納入年齡60–80歲、經(jīng)臨床及β-淀粉樣蛋白PET-CT確診的中重度AD患者。受試者隨機(jī)分為兩組:實(shí)驗(yàn)組接受ABSCs聯(lián)合生長(zhǎng)因子(BDNF、VEGF、IGF-1)靜脈輸注;對(duì)照組僅接受標(biāo)準(zhǔn)藥物治療。ABSCs取自患者外周血,經(jīng)密度梯度離心與流式細(xì)胞術(shù)鑒定后新鮮制備,于3小時(shí)內(nèi)回輸,不予體外擴(kuò)增。生長(zhǎng)因子按標(biāo)準(zhǔn)化劑量配制。全療程共進(jìn)行3次輸注,每次間隔4周。
評(píng)估指標(biāo)與數(shù)據(jù)分析
療效與機(jī)制評(píng)估采用多層面、縱向的設(shè)計(jì):
- 臨床結(jié)局:主要使用簡(jiǎn)易精神狀態(tài)檢查量表、臨床癡呆評(píng)定量表-總分和阿爾茨海默病評(píng)估量表-認(rèn)知子量表,在基線、治療后3個(gè)月和6個(gè)月評(píng)估認(rèn)知功能。
- 神經(jīng)影像學(xué)生物標(biāo)志物:在基線和治療后6個(gè)月,通過(guò)淀粉樣蛋白PET-CT(量化Centiloid值)、氟代脫氧葡萄糖-PET(評(píng)估腦代謝)和磁共振成像(測(cè)量海馬體積)來(lái)評(píng)估大腦病理與結(jié)構(gòu)變化。
- 分子機(jī)制探索:通過(guò)酶聯(lián)免疫吸附測(cè)定檢測(cè)血漿炎癥因子水平;通過(guò)蛋白質(zhì)印跡法分析外周血單核細(xì)胞中PI3K/Akt、MAPK/ERK等信號(hào)通路關(guān)鍵蛋白的磷酸化與表達(dá)水平。
- 安全性監(jiān)測(cè):全程記錄和分類(lèi)不良事件,并定期進(jìn)行實(shí)驗(yàn)室檢查。
- 統(tǒng)計(jì)分析:采用描述性統(tǒng)計(jì)總結(jié)基線特征。主要使用配對(duì)t檢驗(yàn)進(jìn)行組內(nèi)前后比較,使用獨(dú)立樣本t檢驗(yàn)或Mann-Whitney U檢驗(yàn)進(jìn)行組間比較。對(duì)于縱向重復(fù)測(cè)量數(shù)據(jù)(如影像學(xué)和分子數(shù)據(jù)),采用線性混合效應(yīng)模型進(jìn)行分析。
參與患者及其特征
本研究共納入38例中重度AD患者,隨機(jī)分配至實(shí)驗(yàn)組(23例,接受ABSCs聯(lián)合生長(zhǎng)因子治療)和對(duì)照組(15例,接受標(biāo)準(zhǔn)藥物治療)。兩組受試者的基線特征具有可比性,在年齡、性別、疾病嚴(yán)重程度和認(rèn)知評(píng)分方面均無(wú)顯著差異(表1)。平均年齡72.3歲,女性占比60%,以中度AD為主。
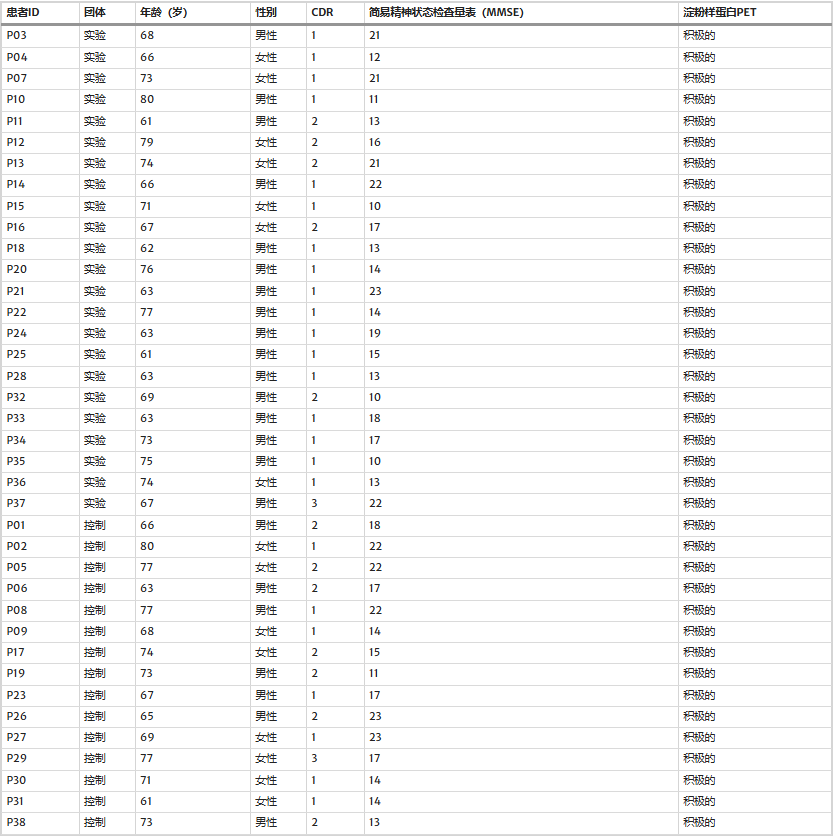
兩組在年齡、性別、疾病嚴(yán)重程度及基線認(rèn)知評(píng)分等方面均具可比性(p>0.05)。所有受試者均完成全部治療及3個(gè)月、6個(gè)月隨訪,無(wú)脫落病例,數(shù)據(jù)完整性良好(圖1)。
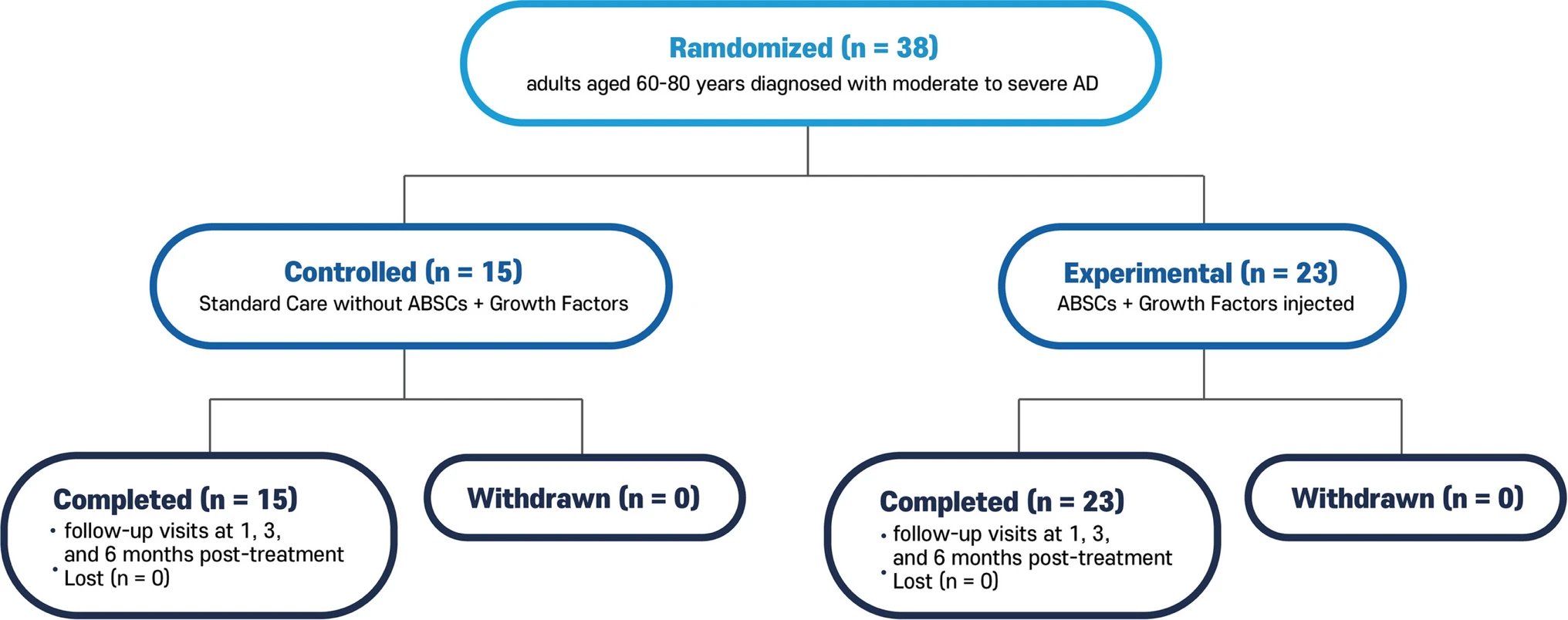
對(duì)照組均接受穩(wěn)定的標(biāo)準(zhǔn)藥物治療(如乙酰膽堿酯酶抑制劑和/或美金剛),且在入組前至少12周及研究期間方案保持不變。研究者指出,盡管兩組基線嚴(yán)重程度經(jīng)調(diào)整后可比,但患者間仍存在一定異質(zhì)性,未來(lái)研究可采用分層隨機(jī)以提高組間同質(zhì)性。
ABSCs治療改善了阿爾茨海默病患者認(rèn)知功能的具體表現(xiàn)
根據(jù)研究數(shù)據(jù),ABSCs聯(lián)合生長(zhǎng)因子治療對(duì)阿爾茨海默病患者的認(rèn)知功能改善表現(xiàn)在以下三個(gè)方面,且改善具有統(tǒng)計(jì)顯著性和較大的效應(yīng)量:
第一,在整體認(rèn)知狀態(tài)方面,治療顯著提升了患者的MMSE評(píng)分(圖2A)。實(shí)驗(yàn)組患者的MMSE平均分在治療3個(gè)月后即顯著增加3.4分,并在6個(gè)月時(shí)進(jìn)一步提升至比基線高4.1分。相比之下,對(duì)照組的分?jǐn)?shù)在整個(gè)研究期間無(wú)顯著變化。兩組改善程度的差異具有很大的效應(yīng)量,且統(tǒng)計(jì)分析證實(shí)了治療與時(shí)間之間存在顯著的交互作用,表明認(rèn)知提升是治療帶來(lái)的持續(xù)效果。
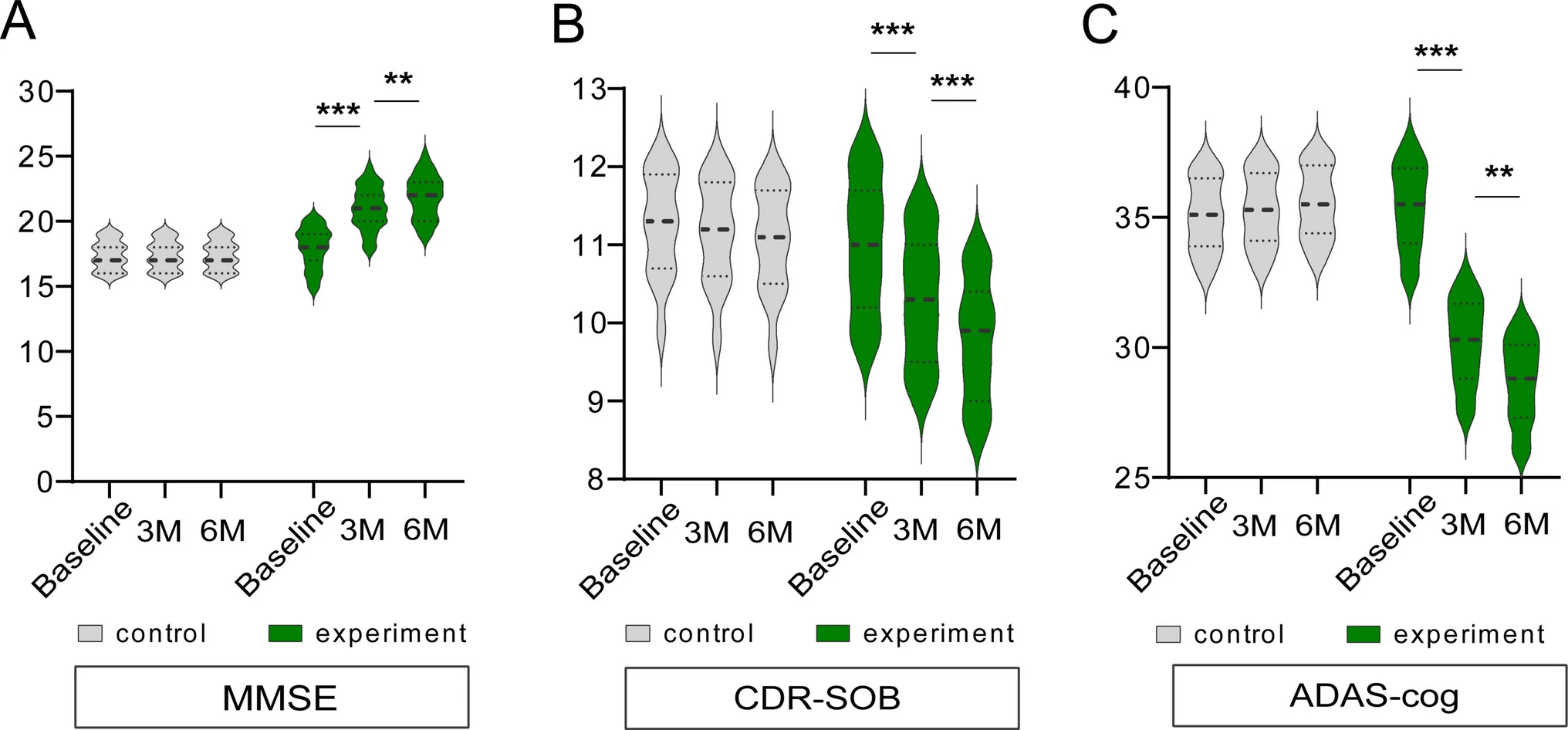
第二,在日常功能障礙方面,治療有效降低了標(biāo)志病情嚴(yán)重的CDR-SOB評(píng)分(圖2B)。實(shí)驗(yàn)組患者的CDR-SOB評(píng)分在治療后持續(xù)下降,至6個(gè)月時(shí)較基線顯著降低了0.9分,意味著日常功能有所改善。而對(duì)照組評(píng)分無(wú)顯著變化。此改善同樣具有中到大的效應(yīng)量,并得到統(tǒng)計(jì)模型的顯著支持,證實(shí)了治療對(duì)減緩功能衰退的有效性。
第三,在阿爾茨海默病核心認(rèn)知癥狀方面,治療使專(zhuān)用的ADAS-Cog評(píng)分顯著下降(圖3)。實(shí)驗(yàn)組患者的ADAS-Cog評(píng)分在6個(gè)月時(shí)較基線大幅下降了6.4分,顯示記憶、語(yǔ)言等核心認(rèn)知領(lǐng)域得到改善。對(duì)照組同期評(píng)分則略有上升。兩組變化的差異同樣具有很大的效應(yīng)量,統(tǒng)計(jì)模型再次確認(rèn)了治療隨時(shí)間的顯著益處,證明了其對(duì)延緩疾病特異性認(rèn)知衰退的積極作用。
自體干細(xì)胞治療的阿爾茨海默病患者生長(zhǎng)因子與生存信號(hào)通路活性增強(qiáng)
在ABSCs聯(lián)合生長(zhǎng)因子治療阿爾茨海默病患者中,生長(zhǎng)因子與生存信號(hào)通路活性增強(qiáng)的核心表現(xiàn)為關(guān)鍵神經(jīng)保護(hù)通路的顯著激活以及突觸相關(guān)蛋白的上調(diào)。
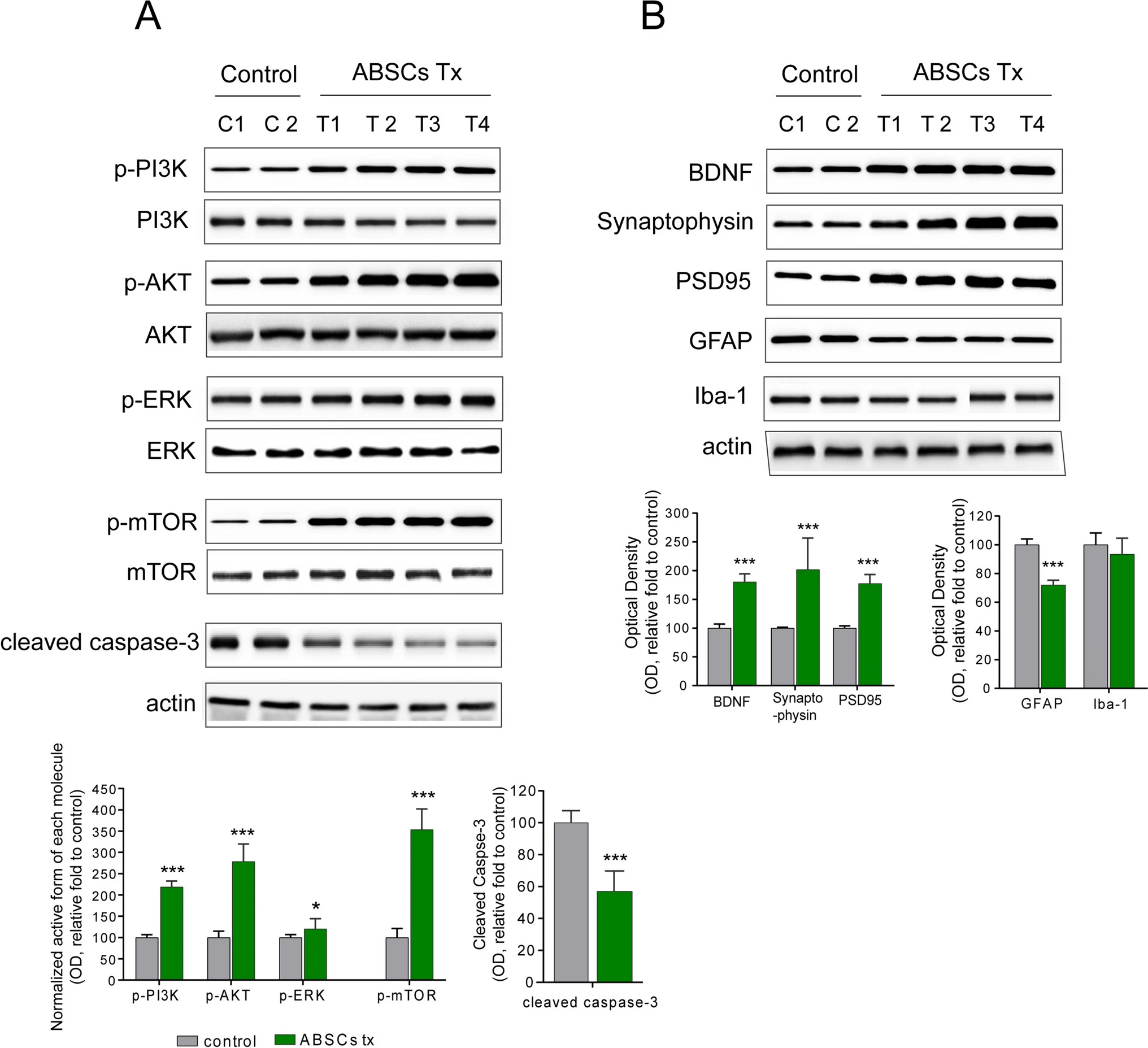
治療后6個(gè)月,實(shí)驗(yàn)組患者外周血中磷酸化Akt(p-Akt)和磷酸化ERK(p-ERK)的水平較基線分別大幅提升32.1%和28.4%,表明PI3K/Akt和MAPK/ERK這兩條核心的細(xì)胞存活與神經(jīng)保護(hù)信號(hào)通路被有效激活(圖3A)。
與此同時(shí),直接反映神經(jīng)可塑性與突觸功能的神經(jīng)營(yíng)養(yǎng)因子BDNF以及突觸標(biāo)志蛋白(突觸素和PSD95)的表達(dá)水平也同步顯著升高,共同證實(shí)了治療在分子層面強(qiáng)化了促生存與神經(jīng)修復(fù)的信號(hào)網(wǎng)絡(luò)(圖3B)。
此外,生存信號(hào)通路活性的增強(qiáng)伴隨著神經(jīng)炎癥環(huán)境的顯著改善,間接支持了其神經(jīng)保護(hù)效應(yīng)。實(shí)驗(yàn)組中,代表星形膠質(zhì)細(xì)胞活化的GFAP蛋白表達(dá)被顯著抑制,同時(shí)促炎細(xì)胞因子TNF-α、IL-6和IL-1β的血漿水平在治療后6個(gè)月分別下降23.6%± 8.7%、21.3%±6.4%和18.7%±7.1%。這種炎癥反應(yīng)的減輕與生存通路的激活、以及小膠質(zhì)細(xì)胞標(biāo)志物Iba-1的下調(diào)趨勢(shì)相一致,整體勾勒出一個(gè)從分子信號(hào)到細(xì)胞環(huán)境全面轉(zhuǎn)向支持神經(jīng)元存活與功能的良性改變(圖4)。
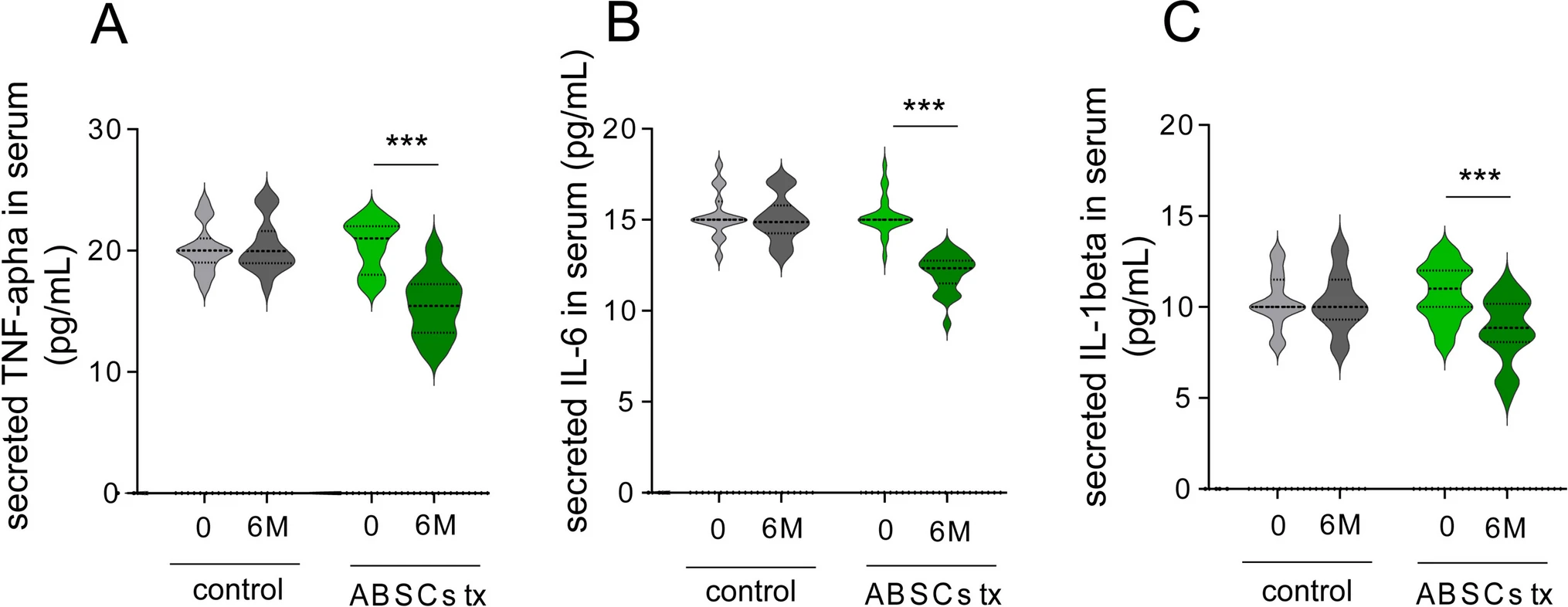
ADSCs治療阿爾茨海默病患者的神經(jīng)影像學(xué)結(jié)果
根據(jù)神經(jīng)影像學(xué)評(píng)估結(jié)果,自體干細(xì)胞治療對(duì)阿爾茨海默病患者的大腦產(chǎn)生了多層面的積極影響,具體表現(xiàn)如下:
淀粉樣蛋白負(fù)荷減輕:首先,在疾病核心病理層面,淀粉樣蛋白PET-CT掃描顯示治療顯著降低了大腦的淀粉樣斑塊負(fù)荷。治療后6個(gè)月,實(shí)驗(yàn)組的平均Centiloid值較基線大幅下降了32.4單位,而對(duì)照組未見(jiàn)顯著變化。這表明治療可能直接干預(yù)了阿爾茨海默病的標(biāo)志性病理進(jìn)程,提示其具有潛在的疾病修飾作用(圖5A)。
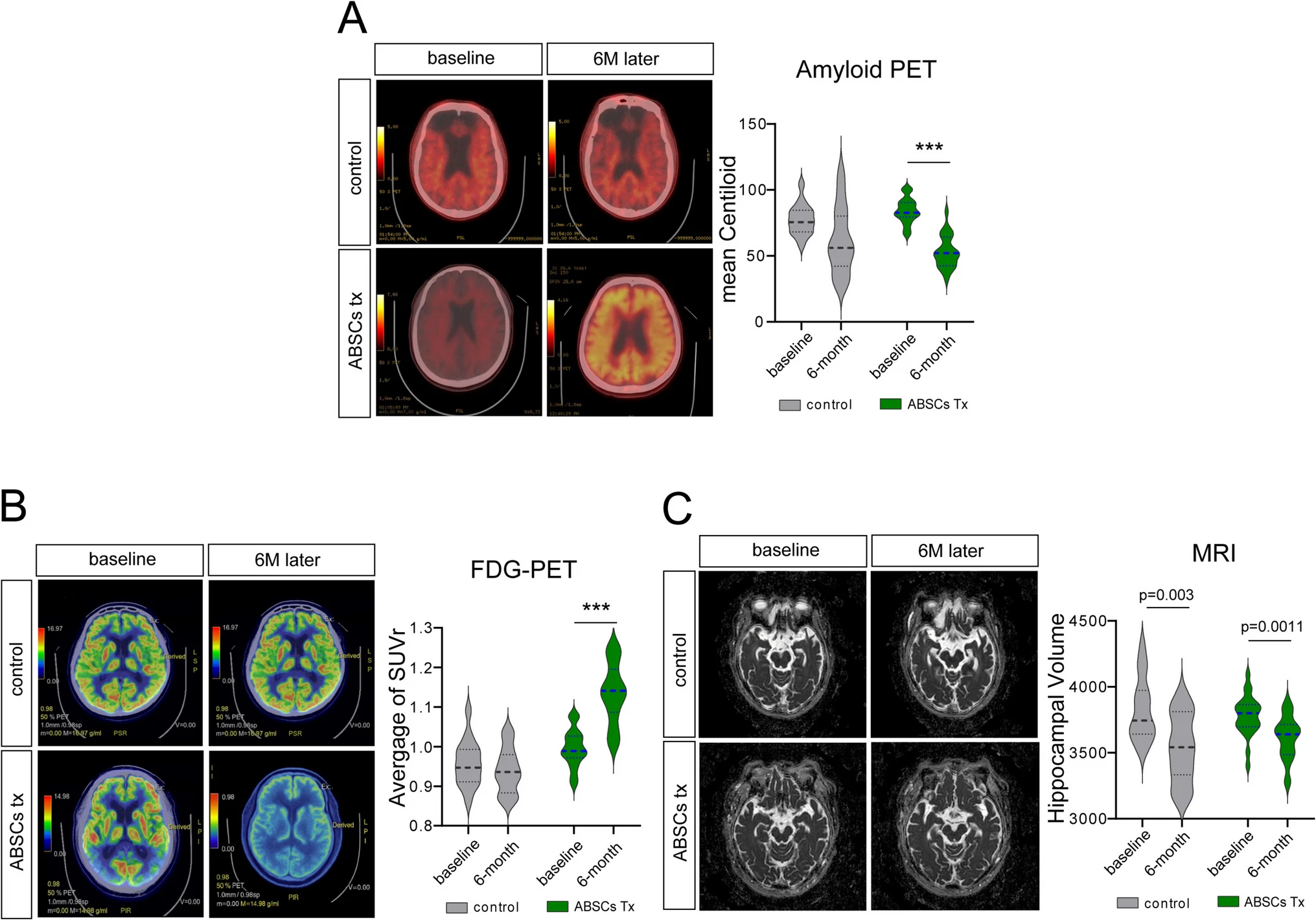
腦代謝活動(dòng)增強(qiáng):其次,在大腦功能代謝層面,F(xiàn)DG-PET結(jié)果顯示關(guān)鍵腦區(qū)的葡萄糖代謝得到顯著增強(qiáng)。實(shí)驗(yàn)組在海馬體和頂葉皮層等區(qū)域的標(biāo)準(zhǔn)化攝取值比率平均提升了14.6%,意味著神經(jīng)元活動(dòng)和能量代謝獲得改善。相比之下,對(duì)照組的腦代謝水平則呈輕微下降趨勢(shì)(圖5B)。
海馬萎縮延緩:第三,在腦結(jié)構(gòu)保護(hù)層面,MRI掃描證實(shí)治療減輕了海馬體的萎縮速度。治療6個(gè)月后,實(shí)驗(yàn)組海馬體積的萎縮率(平均減少4.3%)顯著低于對(duì)照組(7.9%)。這一結(jié)構(gòu)上的保護(hù)效應(yīng)為治療的神經(jīng)保護(hù)作用提供了直接的影像學(xué)證據(jù)(圖5C)。
最后,需要謹(jǐn)慎解讀的是,盡管觀察到的淀粉樣蛋白減少幅度遠(yuǎn)超測(cè)量誤差和疾病自然進(jìn)展速度,提示了積極的生物學(xué)效應(yīng),但研究者指出,由于本研究是單中心探索性試驗(yàn),且缺乏多中心標(biāo)準(zhǔn)化的影像校準(zhǔn),目前的結(jié)果仍屬于初步發(fā)現(xiàn)。未來(lái)需要更大樣本、采用標(biāo)準(zhǔn)化流程的研究來(lái)驗(yàn)證這些影像學(xué)改變的可靠性和可重復(fù)性。
安全性概況和不良事件
在本研究中,自體干細(xì)胞(ABSC)聯(lián)合生長(zhǎng)因子療法的安全性良好,未報(bào)告嚴(yán)重不良事件(SAE)。觀察到的最常見(jiàn)副作用均為短暫性,包括干細(xì)胞輸注后的疲勞和低熱,這通常表明基于干細(xì)胞的干預(yù)措施安全且耐受性良好。
重要的是,未觀察到免疫排斥、腫瘤發(fā)生或其他嚴(yán)重并發(fā)癥的證據(jù),進(jìn)一步證實(shí)了基于ABSC的治療在阿爾茨海默病(AD)中的安全性。
本研究中使用的生長(zhǎng)因子,以及已發(fā)表的在神經(jīng)退行性疾病或血管疾病中使用類(lèi)似劑量生長(zhǎng)因子的I/II期臨床試驗(yàn),均顯示出可接受的安全性,這為本探索性臨床試驗(yàn)采用保守的給藥策略提供了理論依據(jù)。
討論與探討其詳情機(jī)制
本研究初步證實(shí),ABSCs聯(lián)合生長(zhǎng)因子治療可能通過(guò)神經(jīng)保護(hù)與癥狀改善雙重機(jī)制對(duì)中重度AD患者產(chǎn)生積極影響。治療不僅在認(rèn)知功能、淀粉樣斑塊負(fù)荷及神經(jīng)影像指標(biāo)上表現(xiàn)出顯著改善,還可調(diào)節(jié)與神經(jīng)保護(hù)、炎癥反應(yīng)相關(guān)的關(guān)鍵分子通路。
這些發(fā)現(xiàn)為長(zhǎng)期以來(lái)缺乏有效疾病修飾治療的AD提供了一種新的潛在策略。以下將就機(jī)制、與近期研究的對(duì)比及未來(lái)方向展開(kāi)探討。
自體干細(xì)胞聯(lián)合生長(zhǎng)因子治療阿爾茨海默病的主要機(jī)制
自體干細(xì)胞(ABSC)聯(lián)合生長(zhǎng)因子治療阿爾茨海默病的主要機(jī)制是一個(gè)多靶點(diǎn)協(xié)同作用的過(guò)程,可歸納為以下三個(gè)方面:
首先,治療的核心機(jī)制在于顯著激活了細(xì)胞內(nèi)的關(guān)鍵生存與神經(jīng)保護(hù)信號(hào)通路。研究證實(shí),PI3K/Akt和MAPK/ERK這兩條對(duì)神經(jīng)元存活、抗凋亡及突觸可塑性至關(guān)重要的通路被強(qiáng)烈激活,表現(xiàn)為磷酸化Akt(p-Akt)和磷酸化ERK(p-ERK)水平顯著升高。這些通路的激活如同啟動(dòng)了神經(jīng)元內(nèi)部的“生存程序”,直接對(duì)抗退行性病變,為后續(xù)的修復(fù)奠定分子基礎(chǔ)。
其次,治療通過(guò)上調(diào)關(guān)鍵神經(jīng)營(yíng)養(yǎng)因子并增強(qiáng)突觸完整性,直接支持神經(jīng)修復(fù)與可塑性。被激活的通路進(jìn)一步促進(jìn)了腦源性神經(jīng)營(yíng)養(yǎng)因子(BDNF)、胰島素樣生長(zhǎng)因子-1(IGF-1)和血管內(nèi)皮生長(zhǎng)因子(VEGF)等的表達(dá)。這些因子分別發(fā)揮促進(jìn)神經(jīng)元存活、支持海馬區(qū)神經(jīng)生長(zhǎng)以及維護(hù)腦血管健康的作用。同時(shí),突觸標(biāo)志蛋白(如突觸素和PSD95)的上調(diào),從結(jié)構(gòu)上證實(shí)了突觸功能的強(qiáng)化,這很可能是患者認(rèn)知功能獲得改善的直接細(xì)胞基礎(chǔ)。
最后,治療發(fā)揮了強(qiáng)大的免疫調(diào)節(jié)與抗炎作用,為大腦創(chuàng)造了有利的修復(fù)環(huán)境。阿爾茨海默病腦中過(guò)度活化的神經(jīng)炎癥會(huì)加速損傷。本研究顯示,治療后促炎細(xì)胞因子(如TNF-α、IL-6)水平顯著下降,同時(shí)活化星形膠質(zhì)細(xì)胞的標(biāo)志物GFAP也明顯減少。這表明干細(xì)胞療法有效抑制了有害的神經(jīng)炎癥反應(yīng),減輕了炎癥對(duì)神經(jīng)元的持續(xù)攻擊,從而間接保護(hù)了腦組織。
綜上所述,該療法通過(guò)“激活生存信號(hào)-提供營(yíng)養(yǎng)支持-抑制有害炎癥”三位一體的協(xié)同機(jī)制,共同減緩神經(jīng)變性、促進(jìn)修復(fù),最終實(shí)現(xiàn)了延緩疾病進(jìn)展和改善認(rèn)知功能的效果。
結(jié)論與展望
這項(xiàng)臨床試驗(yàn)證實(shí)了將自體干細(xì)胞(ABSC)與生長(zhǎng)因子聯(lián)合用于治療中重度阿爾茨海默病(AD)患者的療效。
該療法顯著改善了患者的認(rèn)知功能,減少了淀粉樣斑塊負(fù)荷,并改善了神經(jīng)影像學(xué)結(jié)果,表明這種新型療法不僅能夠緩解癥狀,還能改變潛在的疾病進(jìn)程。關(guān)鍵分子通路,例如PI3K/Akt和MAPK/ERK通路,得到了有利的調(diào)節(jié),從而促進(jìn)了神經(jīng)元存活、神經(jīng)保護(hù)和神經(jīng)可塑性。這些發(fā)現(xiàn)凸顯了該療法靶向神經(jīng)退行性疾病多種機(jī)制以實(shí)現(xiàn)全面治療獲益的潛力。
研究中未出現(xiàn)嚴(yán)重不良事件,提示該聯(lián)合方案耐受性良好,具備進(jìn)一步臨床推廣的安全性基礎(chǔ)。未來(lái)需開(kāi)展更大樣本、多中心、長(zhǎng)期隨訪的隨機(jī)對(duì)照試驗(yàn),以驗(yàn)證其持久療效與疾病修飾作用,并探索最佳治療時(shí)機(jī)、劑量及人群分層策略。
參考資料:[1]:Lee, W.J., Cho, K., Lee, D. et al. Therapeutic Efficacy of Autologous Blood-Derived Stem Cells with Growth Factors in Moderate to Severe Alzheimer’s Disease: A Clinical Trial. Mol Neurobiol 63, 277 (2026). https://doi.org/10.1007/s12035-025-05583-0
免責(zé)說(shuō)明:本文僅用于傳播科普知識(shí),分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專(zhuān)業(yè)建議。如有版權(quán)等疑問(wèn),請(qǐng)隨時(shí)聯(lián)系我。



 掃碼添加官方微信
掃碼添加官方微信